ATOMO
L' ATOMO E' LA PIU'
PICCOLA PARTE DELLA MATERIA, INVISIBILE AD OCCHIO NUDO E ANCHE AL MICROSCOPIO. OGNI
COSA E' COMPOSTA DA ATOMI. QUESTI SONO COMPOSTI DAL NUCLEO LA CUI GRANDEZZA E'
MINIMA: PUO' ESSERE PARAGONATO AD UNA PALLINA DA PING PONG IN UNO STADIO DA
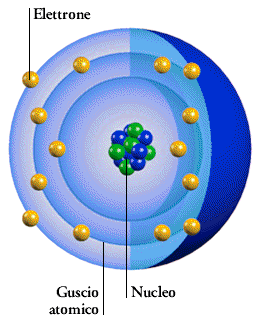
CALCIO. ALL'INTERNO DEL NUCLEO SI TROVANO I PROTONI, CON CARICA ELETTRICA
POSITIVA E I NEUTRONI, SENZA CARICA ELETTRICA. ATTORNO AL NUCLEO RUOTANO SENZA
UN'ORBITA PRESTABILITA GLI ELETTRONI, CON CARICA ELETTRICA NEGATIVA E LA CUI
MASSA E' 3600 VOLTE MINORE A QUELLA DI PROTONI E NEUTRONI. GLI ELETTRONI NON SI
ALLONATANANO MAI DAL NUCLEO, QUESTO PERCHE' SONO ATTRATTI DALLE CARICHE
ELETTRICHE POSITIVE DEI PROTONI, INFATTI UN PRINCIPIO DELL' ELETTROSTATICA
AFFERMA CHE CARICHE DI UGUALE SEGNO SI RESPINGONO E CARICHE DI SEGNO OPPOSTO SI
ATTRAGGONO. E' GRAZIE A QUESTO PRINCIPIO CHE GLI ELEMENTI DELLA TERRA TENGONO
INSIEME COSI' DA FORMARE TUTTO CIO' CHE CI CIRCONDA.
IL NUMERO
DEI PROTONI DI UN ATOMO COSTITUISCE IL NUMERO ATOMICO DELL’ELEMENTO, IL
NUMERO DEI PROTONI E DEI NEUTRONI COSTITUISCE INVECE IL NUMERO DI MASSA. DELLE
ECCEZIONI ALLE REGOLE SONO GLI ISOTOPI:
ATTORNO AL NUCLEO GLI ELETTRONI SONO DISPOSTI SU GUSCI CONCENTRICI CHIAMATI ORBITALI: IL PRIMO PUO’ CONTENERE AL MASSIMO 2 ELETTRONI, IL SECONDO 8 ELETTRONI E IL TERZO ANCHE. GLI ATOMI TUTTAVIA TENDONO A VOLER COMPLETARE IL LORO GUSCIO PIU’ESTERNO E PERCIO’ CEDONO E ACQUISTANO ELETTRONI CON GLI ATOMI VICINI CHE FORMANO LO STESSO ELEMENTO O COMPOSTO CHIMICO. AD ESEMPIO NEL METANO (CH4) L’ATOMO DI CARBONIO CHE HA 4 ELETTRONI SULL’ORBITALE PIU’ ESTERNO, ACQUISTA I 4 ELETTRONI DEGLI ALTRI 4 ATOMI DI IDROGENO, COSI’ DA COMPLETARE IL SUO ULTIMO GUSCIO. ESISTONO TUTTAVIA GAS (DETTI NOBILI) CHE AVENDO L’ORBITALE ESTERNO COMPLETO NON HANNO BISOGNO DI FARE ULTERIORI SCAMBI.
UNA SCIENZA CHE
STUDIA IL FENOMENO DELL’ACCUMULO DELLE CARICHE ELETTRICHE E’ L’ELETTROSTATICA
(UN RAMO DELL’ELETTROLOGIA).
FENOMENO
IMPORTANTE IN QUESTO CONTESTO E’ IL MAGNETISMO.